Aptima™ HCV Quant Dx Assay
Nachweis einer aktiven Infektion und Monitoring der Hepatitis-C-Viruslast (HCV).1

Sensitiver Nachweis
Der Test liefert präzise Ergebnisse für alle wichtigen Genotypen. Er bietet eine hervorragende Sensitivität und hohe Präzision, selbst bei Proben mit geringer Viruslast.1 Die Kombination aus dem Aptima HCV Quant Dx Assay und dem Panther® System vereint eine überlegene Testleistung mit erstklassiger Automatisierung von der Probe bis zum Ergebnis in einem einzigen System.1
Effizienter Workflow und flexible Verarbeitung
Probenflexibilität durch die Validierung für EDTA-, Plasmavorbereitungs- (PPT) und ACD-Röhrchen.1 Ermöglicht die Durchführung mehrerer Tests mit nur einer Probe. Keine manuelle Probenvorbereitung bei Beladung mit Primärröhrchen, sodass Verwechselungen ausgeschlossen sind.
Random Access und schnelle Ergebnisse
Batch-Verarbeitung ist Vergangenheit. Sie können verschiedene Tests an ein- und derselben Probe auswählen, sobald diese im Labor angekommen ist. Schnelle Bearbeitungszeit – erste Ergebnisse in nur 2 Stunden und 41 Minuten. STAT-Priorisierung.2
Automatische Analyse und automatischer Verdünnungsfaktor
Automatisierte QC-Analyse mit Levey-Jennings-Diagrammen zur Verfolgung und Trendermittlung von Kontrollen. Option für geringes Probenvolumen (240 μl) inklusive eines automatischen Verdünnungsfaktors mit anschließender Verwendung dieses Faktors anstelle von manuellen Berechnungen.1,2
Einfachere und skalierbare Diagnostik
Der Aptima HCV Quant Dx Assay ist Teil der Molecular Scalable Solution von Hologic – ein Portfolio, das ein breites, leistungsstarkes Testmenü mit Hochdurchsatz-Automatisierung vereint. Konzipiert zur flexiblen Skalierung gemäß Ihren Anforderungen, von Einzeltestungen bis zum breiten Screening der Bevölkerung.

Exzellente Sensitivität und hohe Präzision
Selbst bei Proben mit geringer Viruslast.1
4,3 IU/ml
Plasma
Nachweisgrenze (LoD)
3,9 IU/ml
Serum
Nachweisgrenze (LoD)
10 IU/ml*
Untere Bestimmungsgrenze (LLoQ)
10-100 Mio. IU/ml
Linearer Bereich
Neue Maßstäbe1 für HCV-Tests
- Verwendungszweck: Nachweis einer aktiven Infektion und Monitoring der Viruslast
- Technologie: Real-Time-transkriptionsvermittelte Amplifikation (TMA)
- Target-Region: Hoch konservierte Region von HCV-RNA (5’ UTR)
- Genotypen: 1-6
- Probentypen: Plasma und Serum

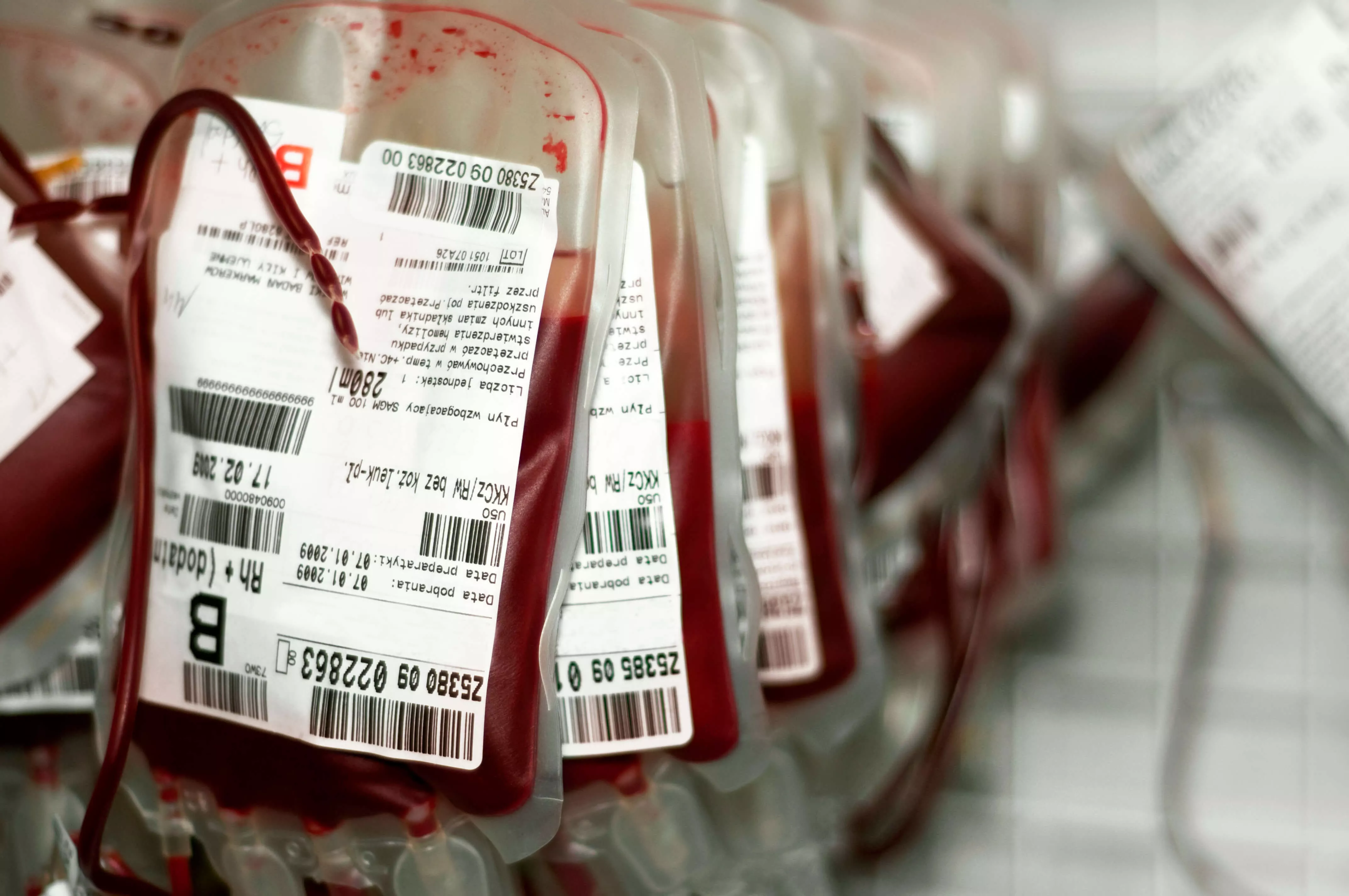
Verbesserung der Behandlung
HCV ist ein blutübertragbarer Erreger und weltweit eine Belastung für Gesundheitssysteme. Bis zu 170 Millionen Menschen sind infiziert, und jährlich sterben 350.000 an HCV-bedingten Erkrankungen.3,4 Die Quantifizierung der HCV-RNA (Viruslast) ist zentral für die Bestimmung des Erregers und das Monitoring des Therapieerfolgs. Ein anhaltendes virologisches Ansprechen (SVR) zeigt sich durch nicht nachweisbare HCV-RNA nach der Therapie.5,6 Im Zeitalter direkt wirkender antiviraler Arzneimittel (DAA) wird die Viruslast vor, während und nach der Therapie gemessen, um den Ausgangswert, das Ansprechen und das SVR (oder einen Rückfall) zu bewerten.4-6
Evidenz. Einblicke. Zusammenarbeit.
Unser Bildungsportal verbessert die Patientenversorgung durch hervorragende Schulungen, die Vermittlung klinischer und wissenschaftlicher Fakten sowie Partnerschaften mit den medizinischen Fachkreisen.
Einblicke
*Die LLoQ wurde genotypübergreifend ermittelt (siehe Packungsbeilage „Ermittlung der unteren Bestimmungsgrenze (LLoQ) für verschiedene HCV-Genotypen“). Diese Genotypdaten ergeben für den Test eine allgemeine LLoQ von 10 IU/ml.
Aptima HCV Quant Dx Assay [Packungsbeilage] AW-13249-001. Rev.005 San Diego, CA; Hologic, Inc., 2019.
Panther / Panther Fusion Bedienungsanleitung AW-26055-001 Rev. 001
Averhoff FM, Glass N and Holtzman D. Global Burden of Hepatitis C: Considerations for Healthcare Providers in the United States. Clinical Infectious Diseases 2012; 55 (S1): S10-15.
Current and Future Disease Progression of the Chronic HCV Population in the United States (2013) PLOS ONE Band 8: 5. Ausgabe; 1-10.
Rutter, K, Hofer H, Beinhardt, S et al., Durability of SVR in chronic hepatitis C patients treated with peginterferon-α2a/ribavirin in combination with a direct acting antiviral. Aliment Pharmacol Ther. 2013 Jul;38(2):118-23.
Kohli A, Shaffer A, Sherman A, et al. Treatment of Hepatitis C, A Systemic Review (2014) JAMA 2014 Aug 13;312(6): 631-640.
Dokumente
Sicherheitsdatenblätter
Packungsbeilagen
Zugehörige Produkte
1434
Hologic BV, Da Vincilaan 5, 1930 Zaventem, Belgium.
Kennnummer wo zutreffend